La médecine intégrative
De quoi parle t-on ?
Elle croise tout ce qui est connu, de la biologie de la tumeur et de son environnement, ainsi que toutes les disciplines disponibles (intelligence artificielle, imagerie médicale, réalité virtuelle) pour mieux définir la stratégie thérapeutique adaptée.
Ce qui se profile d'ici 2030
La médecine intégrative permet la construction d'un nouvel atlas du cancer résumant toutes les connaissances dans une perspective thérapeutique et intégrative.
Cette construction, pierre à pierre, vise à teinter l'ancienne approche statistique du traitement du cancer d'une approche personnalisée, prenant en compte à la fois des expériences spécifiques et le malade dans sa globalité.
Aujourd'hui, 97 % de la population atteinte de cancer est traitée par ce qui est démontré chez 3 % des patients.
Toutes les inconnues dues à l'hétérogénéité des patients ont été confinées derrière les données statistiques de manière à pouvoir prendre en charge tous les patients.
Petit à petit, les données statistiques vont être complétées par des données biologiques (analyse de la biologie de la tumeur : recherche de mutations, translocations, amplifications, caractérisation des cellules immunitaires infiltrantes), des rapports entre la tumeur et son environnement, afin de mieux sélectionner les patients éligibles à certains traitements, mieux déterminer les doses à administrer et mieux évaluer aussi les risques de rechute.
C'est un changement de prisme qui s'opère en matière de prise en charge du cancer pour écrire des équations intégrant de nouvelles inconnues et fabriquer des médicaments à la carte.
Ce qui est en cours
Le bouleversement du déroulé des essais cliniques
Le paradigme classique de développement de médicament, qui était axé autour de la séquence des phases I, II, et III des essais, se concentre de plus en plus sur le développement précoce de médicament, et la phase I/II.
La phase I/II va au-delà de l'évaluation traditionnelle de la sécurité/toxicité du médicament, elle caractérise l'activité et les biomarqueurs de la réponse et peut inclure jusqu'à 1 000 patients sélectionnés.
La phase I/II a désormais une valeur d'enregistrement et peut mener à une approbation conditionnelle des autorités de santé.
Le bouleversement de la stratégie thérapeutique
Le séquençage de la tumeur et son analyse épigénétique sont de plus en plus souvent utilisés pour déterminer une stratégie thérapeutique tenant compte à la fois de l'hôte, de la tumeur et de leurs interrelations.
La maîtrise de nouveaux outils
On bascule progressivement vers une médecine plus efficace, et le monde médical apprend à maîtriser de nouveaux outils.
Les données et la circulation de ces données (radio, analyse, résultats génétiques...) sont des éléments clés de cette transformation, comme le sera à un peu plus long terme la capacité que nous aurons à collecter cette information, à la stocker et à l'analyser pour pouvoir disposer d'une meilleure connaissance statistique et d'une importante marge de progrès.
On pourra ainsi mieux anticiper l'évolution de la maladie, repérer plus tôt les messages d'alerte et intervenir quand il est temps.
Ce qu'il faut dépasser
Ne pas opposer l'ancien et le nouveau monde : il faut progresser ensemble vers une médecine plus efficiente fondée sur une approche globale.
Ainsi, on peut détecter plus tôt ou anticiper une rechute et économiser des soins lourds, et donc dépenser moins.
Etre efficace, c'est le meilleur moyen d'être économe. La personnalisation à grande échelle permet d'allouer les ressources suffisamment finement pour limiter les surcoûts.
Quelle que soit la stratégie thérapeutique choisie, et aussi fine et précise que puisse être l'analyse en amont de la tumeur et de son environnement, la rémission/guérison d'un cancer dépend aussi de la capacité du patient à faire face à l'annonce et à la cascade d'analyses et de traitements auxquels il va être soumis, à pouvoir compter sur son environnement proche et à être en mesure de réintégrer une vie sociale et professionnelle active après le cancer.
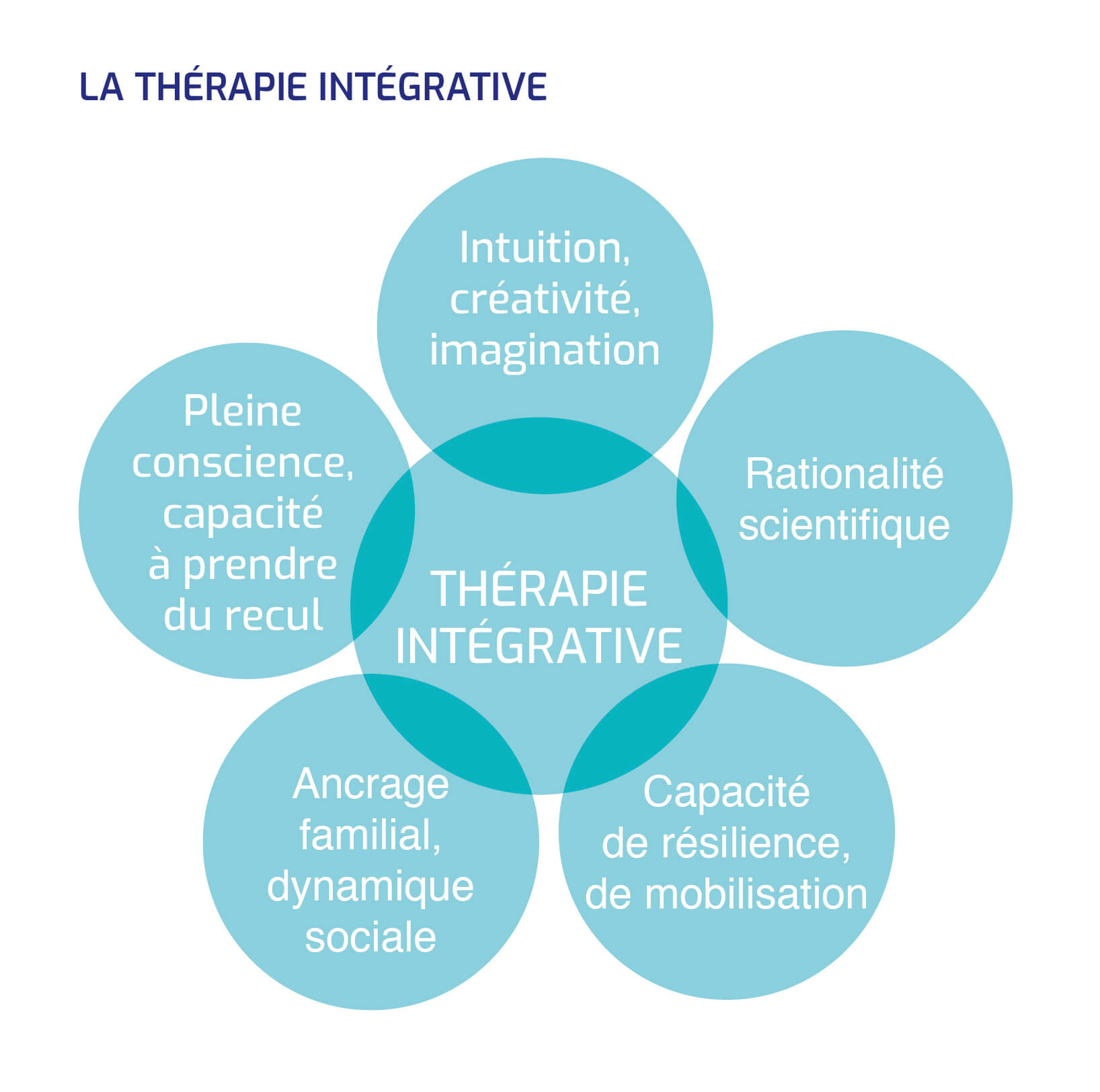
Il faut non seulement considérer la tumeur dans son environnement, mais aussi le patient dans son environnement, avec tous les paramètres qui font sa singularité : sa rationalité, son imagination/intuition, son ancrage familial, sa capacité de résilience et de recul face à la maladie.
Les grands centres américains de lutte contre le cancer ont pris le tournant de la thérapie intégrative dès la fin des années 1990 avec la création de départements de thérapie intégrative au Dana-Farber Cancer Center (Boston), au MD Anderson Cancer Center (Houston), au Memorial Sloan Kettering Center (New York) et au UCSF Osher Center for Integrative Medecine (San Francisco).
Trois centres européens ont été précurseurs, le Karolinska Institutet (Suède), les centres anglais du University College (Londres) et du Christie Hospital (Manchester).
Les centres français (Léon Bérard, Bergonié, Claudius Regaud, Curie, Gustave Roussy, l'AP-HP) ont tous lancé des programmes de thérapie intégrative, que ce soit des ateliers d'art thérapie, de jardinage, de sport, des consultations d'ostéopathie, d'acupuncture, de nutrition...
Seuls, les Osher Centers, qui ont essaimé aux Etats-Unis, ont mis en place un programme d'évaluation de ces thérapies intégratives.
L'institut Rafaël, ouvert en 2018, a pour objectif pionnier d'unir en un même lieu les soins de l'après-cancer :
• les thérapies intégratives dispensées par une équipe de 70 soignants ;
• la recherche et l'évaluation, ainsi que la formation pour structurer un écosystème d'innovation humaniste destiné à mieux s'occuper de chaque individu de façon globale et à favoriser le partage des compétences de chacun.
Fiche réalisée avec l'appui du docteur Alain Toledano, cancérologue radiothérapeute, directeur médical de l'Institut de radiochirurgie de Paris-Centre Hartmann et président de l'Institut Rafaël (www.institut-rafael.fr)
Extrait de Santé 2030 - Partie 2 : les vecteurs d'innovation.
Retrouvez l'intégralité de l'étude sur le site.

